Vordere Kreuzbandruptur
SIE HABEN ODER KENNEN JEMANDEN MIT EINEM VORDEREN KREUZBANDRISS?
Wir fassen auf dieser Seite alle wichtigsten Infos zusammen.
3800 Worte | 18 Minuten Lesezeit
Zuletzt Aktualisiert: Januar 2025
Lieber Kunde, Patient, (Leistungs-) Sportler und/oder (Fach-) Arzt,
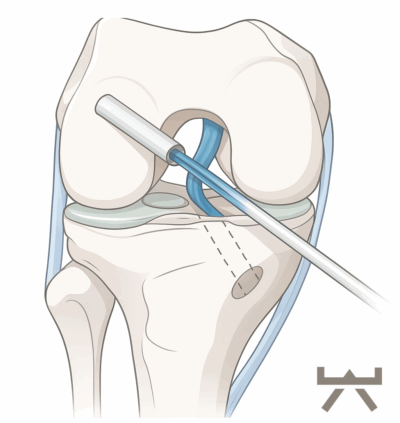
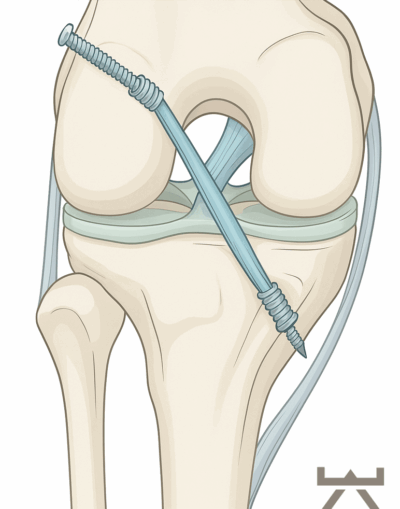
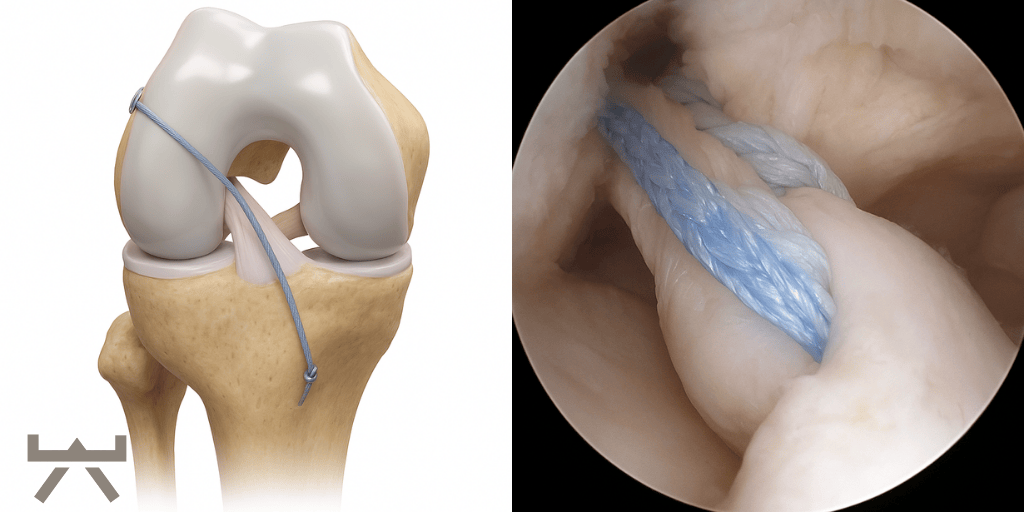
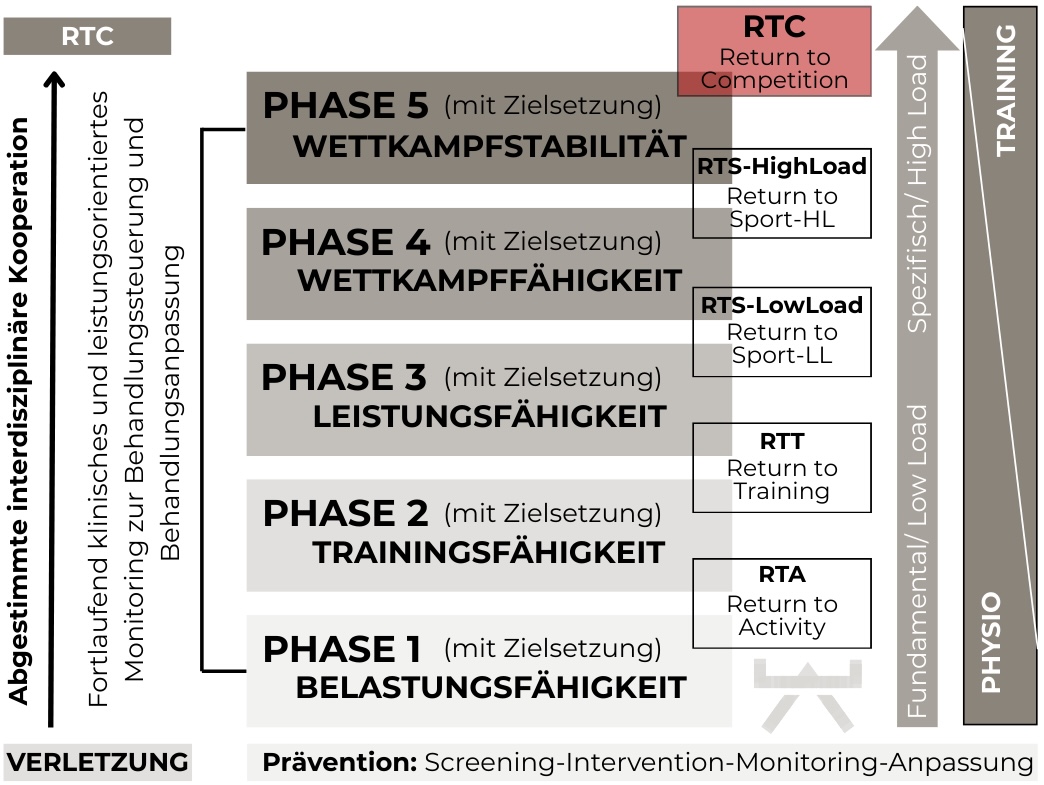
wir wollen Ihnen zu verschiedenen Diagnosen und Verletzungen einen Einblick in die Problematik, unser Vorgehen und unsere Behandlung geben. Hierfür beziehen wir uns auf wissenschaftliche Studien und unsere jahrelange Erfahrung. So können Sie sich schon vorab besser informieren und offene Fragen oder mögliche Unsicherheiten klären. Vordere Kreuzbandverletzungen zählen zu den häufigsten Sportverletzungen des Kniegelenks. Auf 100.000 Einwohner/innen in Europa verletzen sich 81 davon das Kreuzband. Vor allem Sportarten mit plötzlichen Abbrems-/Beschleunigungs- oder Dreh-/Landebewegungen sind anfälliger für eine Verletzung. Umso wichtiger gestaltet sich dem Zufolge die Rehabilitation des Athleten, um Ihn sicher und schnellst möglich wieder in seine Sportart zurückführen zu können und des Weiteren, das Verletzungsrisiko eines erneuten Risses so gering wie möglich zu halten. Wie diese Rehabilitation aussieht, erfahren Sie hier.




Wie die moderne Ernährung dein schön geplantes Leben frühzeitig zur Hölle macht!
Lesezeit: 22 MinutenTeilen: via Twitter auf Facebook auf LinkedIn